การหาลำดับจีโนมทั้งหมด

การแปรผันของโครงสร้างในประชากรจีน และผลกระทบต่อฟีโนไทป์ โรค และการปรับตัวของประชากร
นาโนพอร์ |แพคไบโอ |การจัดลำดับจีโนมใหม่ทั้งหมดการเรียกการเปลี่ยนแปลงโครงสร้าง
ในการศึกษานี้ การจัดลำดับ Nanopore PromethION จัดทำโดย Biomarker Technologies
ไฮไลท์
ในการศึกษานี้ ได้มีการเปิดเผยภาพรวมของการแปรผันของโครงสร้าง (SV) ในจีโนมมนุษย์ด้วยความช่วยเหลือจากการจัดลำดับแบบอ่านยาวบนแพลตฟอร์ม Nanopore PromethION ซึ่งช่วยให้เข้าใจ SV ในด้านฟีโนไทป์ โรค และวิวัฒนาการได้ลึกซึ้งยิ่งขึ้น
การออกแบบการทดลอง
ตัวอย่าง: เม็ดเลือดขาวในเลือดของชาวจีนที่ไม่เกี่ยวข้อง 405 ราย (ชาย 206 รายและหญิง 199 ราย) โดยมีการตรวจวัดทางฟีโนไทป์และทางคลินิก 68 รายการในบรรดาบุคคลทั้งหมด ภูมิภาคบรรพบุรุษของบุคคล 124 คนเป็นจังหวัดทางตอนเหนือ ภูมิภาคของบุคคล 198 คนอยู่ทางใต้ 53 คนอยู่ทางตะวันตกเฉียงใต้ และ 30 คนไม่ทราบ
กลยุทธ์การจัดลำดับ: การจัดลำดับการอ่านแบบยาว (LRS) ของจีโนมทั้งหมดด้วยการอ่าน Nanopore 1D และการอ่าน PacBio HiFi
แพลตฟอร์มการหาลำดับ: Nanopore PromethION;PacBio ภาคต่อ II
การเรียกการเปลี่ยนแปลงโครงสร้าง
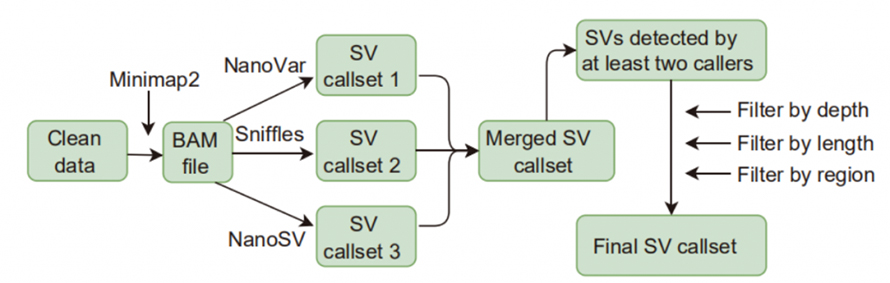
รูปที่ 1 เวิร์กโฟลว์ของการโทรและการกรอง SV
ความสำเร็จหลัก
การค้นพบและการตรวจสอบความแปรผันของโครงสร้าง
ชุดวันที่ของ Nanopore: รวมการอ่านทั้งหมด 20.7 Tb ที่สร้างขึ้นบนแพลตฟอร์มการจัดลำดับ PromethION โดยได้รับข้อมูลเฉลี่ย 51 Gb ต่อตัวอย่างความลึก 17 เท่า
การจัดตำแหน่งจีโนมอ้างอิง (GRCh38): ได้อัตราการแมปเฉลี่ย 94.1%อัตราข้อผิดพลาดเฉลี่ย (12.6%) มีความคล้ายคลึงกับการศึกษาการเปรียบเทียบก่อนหน้า (12.6%) (รูปที่ 2b และ 2c)
การเรียกการเปลี่ยนแปลงโครงสร้าง (SV): ผู้เรียก SV ที่ใช้ในการศึกษานี้ ได้แก่ Sniffles, NanoVar และ NanoSVSV ที่มีความมั่นใจสูงถูกกำหนดให้เป็น SV ที่ระบุโดยผู้โทรอย่างน้อยสองคน และผ่านการกรองตามความลึก ความยาว และภูมิภาค
แต่ละตัวอย่างมีการระบุ SV ที่มีความมั่นใจสูงโดยเฉลี่ย 18,489 รายการ (ตั้งแต่ 15,439 ถึง 22,505)(รูปที่ 2d, 2e และ 2f)
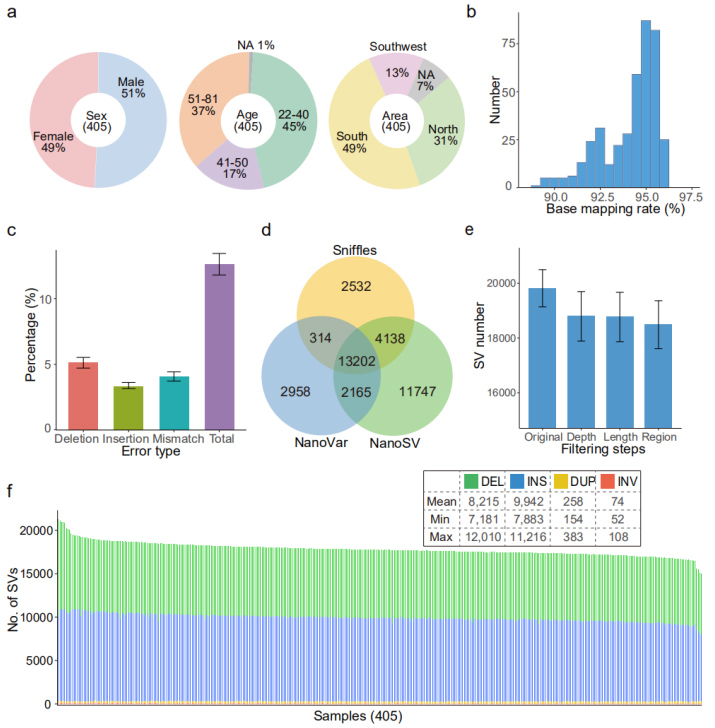
รูปที่ 2 ภาพรวมของ SV ที่ระบุโดยชุดข้อมูล Nanopore
การตรวจสอบโดย PacBio: SV ที่ระบุในหนึ่งตัวอย่าง (HG002, ลูก) ได้รับการตรวจสอบโดยชุดข้อมูล PacBio HiFiอัตราการค้นพบที่ผิดพลาดโดยรวม (FDR) อยู่ที่ 3.2% ซึ่งแสดงให้เห็นการระบุ SV ที่ค่อนข้างเชื่อถือได้โดยการอ่าน Nanopore
SV ที่ไม่ซ้ำซ้อนและคุณสมบัติจีโนม
SV ที่ไม่ซ้ำซ้อน: ชุด SV ที่ไม่ซ้ำซ้อน 132,312 ชุดได้มาจากการรวม SV ไว้ในตัวอย่างทั้งหมด ซึ่งรวมถึง 67,405 DELs, 60,182 INSs, 3,956 DUPs และ 769 INVs(รูปที่ 3ก)
การเปรียบเทียบกับชุดข้อมูล SV ที่มีอยู่: ชุดข้อมูลนี้ถูกเปรียบเทียบกับชุดข้อมูล TGS หรือ NGS ที่เผยแพร่ภายในชุดข้อมูลทั้งสี่ชุดที่เปรียบเทียบกัน LRS15 ซึ่งเป็นชุดข้อมูลเดียวจากแพลตฟอร์มการจัดลำดับแบบอ่านยาว (PacBio) แชร์การทับซ้อนที่ใหญ่ที่สุดกับชุดข้อมูลนี้ยิ่งไปกว่านั้น SV 53.3% (70,471) ในชุดข้อมูลนี้ถูกรายงานเป็นครั้งแรกเมื่อดู SV แต่ละประเภท จำนวน INS ที่กู้คืนด้วยชุดข้อมูลลำดับการอ่านแบบยาวนั้นมากกว่าชุดข้อมูลการอ่านสั้นที่เหลืออย่างมาก ซึ่งบ่งชี้ว่าลำดับการอ่านแบบยาวนั้นมีประสิทธิภาพเป็นพิเศษในการตรวจจับ INS(รูปที่ 3b และ 3c)
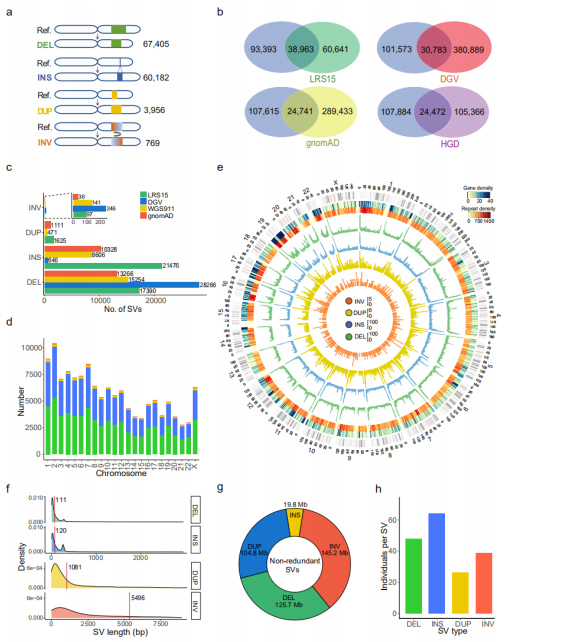
รูปที่ 3 คุณสมบัติของ SV ที่ไม่ซ้ำซ้อนสำหรับ SV แต่ละประเภท
คุณลักษณะทางพันธุกรรม: พบว่าจำนวน SV มีความสัมพันธ์อย่างมีนัยสำคัญกับความยาวของโครโมโซมการกระจายของยีน การทำซ้ำ DELs (สีเขียว), INS (สีน้ำเงิน), DUP (สีเหลือง) และ INV (สีส้ม) ถูกแสดงบนแผนภาพ Circos โดยที่ SV เพิ่มขึ้นโดยทั่วไปที่ปลายแขนโครโมโซม(รูปที่ 3d และ 3e)
ความยาวของ SV: พบว่าความยาวของ INS และ DEL สั้นกว่าความยาวของ DUP และ INV อย่างมาก ซึ่งสอดคล้องกับที่ระบุโดยชุดข้อมูล PacBio HiFiความยาวของ SV ที่ระบุทั้งหมดเพิ่มขึ้นไม่เกิน 395.6 Mb ซึ่งครอบครอง 13.2% ของจีโนมมนุษย์ทั้งหมดSV ส่งผลกระทบต่อจีโนมโดยเฉลี่ย 23.0 Mb (ประมาณ 0.8%) ต่อบุคคล(รูปที่ 3f และ 3g)
ผลกระทบเชิงหน้าที่ ฟีโนไทป์ และทางคลินิกของ SV
การสูญเสียฟังก์ชันที่คาดการณ์ไว้ (pLoF) SV: pLoF SV ถูกกำหนดให้เป็น SV ที่โต้ตอบกับ CDS โดยที่นิวคลีโอไทด์การเข้ารหัสถูกลบหรือ ORF มีการเปลี่ยนแปลงมีคำอธิบายประกอบ pLoF SV ทั้งหมด 1,929 pLoF ที่ส่งผลต่อ CDS จำนวน 1,681 ยีนภายในยีนเหล่านั้น 38 ยีนเน้นที่ "การจับตัวรับอิมมูโนโกลบูลิน" ในการวิเคราะห์การเพิ่มคุณค่า GOpLoF SV เหล่านี้ได้รับการเพิ่มความคิดเห็นเพิ่มเติมโดย GWAS, OMIM และ COSMIC ตามลำดับ(รูปที่ 4a และ 4b)
SV ที่เกี่ยวข้องกับฟีโนไทป์และทางคลินิก: SV จำนวนหนึ่งในชุดข้อมูล nanopore แสดงให้เห็นว่ามีความเกี่ยวข้องทางฟีโนไทป์และทางคลินิกพบ DEL แบบเฮเทอโรไซกัสที่หายากขนาด 19.3 kb ซึ่งทราบกันว่าทำให้เกิดอัลฟาธาลัสซีเมีย ถูกระบุในบุคคล 3 ราย ซึ่งทำให้ยีนของหน่วยย่อยของฮีโมโกลบิน Alpha 1 และ 2 (HBA1 และ HBA2) ทำงานผิดปกติมีการระบุ DEL อีกจำนวน 27.4 kb เกี่ยวกับการเข้ารหัสยีนหน่วยย่อยของฮีโมโกลบินเบต้า (HBB) ในบุคคลอื่นSV นี้เป็นที่ทราบกันว่าทำให้เกิดโรคฮีโมโกลบินผิดปกติอย่างรุนแรง(รูปที่ 4ค)
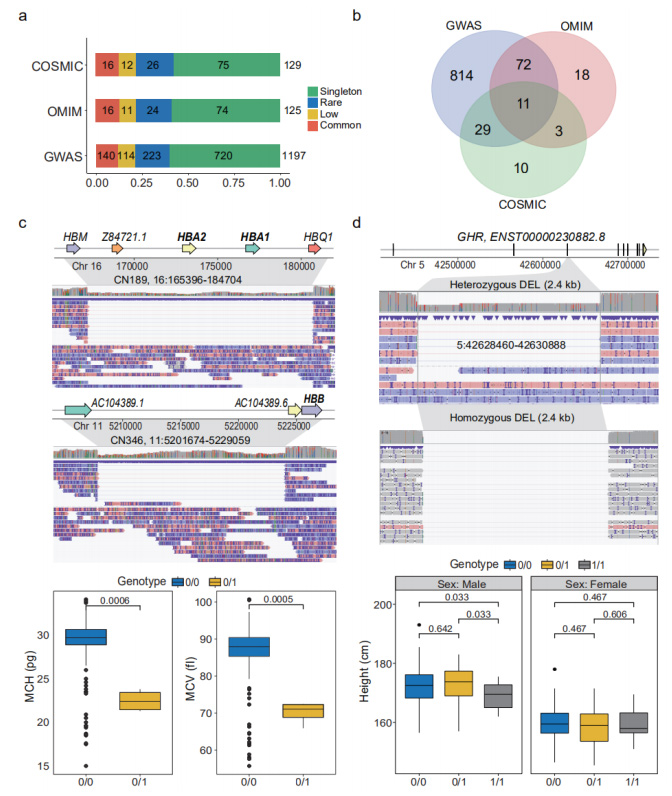
รูปที่ 4 pLoF SVs ที่เกี่ยวข้องกับฟีโนไทป์และโรค
พบ DEL ทั่วไปที่ 2.4 kb ในโฮโมไซกัส 35 ตัวและพาหะเฮเทอโรไซกัส 67 ตัว ซึ่งครอบคลุมพื้นที่ทั้งหมดของ exon ที่ 3 ของ Growth Homone Receptor (GHR)พาหะแบบโฮโมไซกัสพบว่าสั้นกว่าพาหะแบบเฮเทอร์ไซกัสอย่างมีนัยสำคัญ (p=0.033)(รูปที่ 4ง)
นอกจากนี้ SV เหล่านี้ยังได้รับการประมวลผลสำหรับการศึกษาวิวัฒนาการประชากรระหว่างสองกลุ่มภูมิภาค: จีนตอนเหนือและตอนใต้พบการกระจาย SV ที่แตกต่างกันอย่างมีนัยสำคัญใน Chr 1, 2, 3, 6,10,12,14 และ 19 ซึ่งภายในนั้น SV อันดับต้น ๆ เกี่ยวข้องกับขอบเขตภูมิคุ้มกัน เช่น IGH, MHC เป็นต้น มีความสมเหตุสมผลที่จะคาดการณ์ว่า ความแตกต่างใน SV เหล่านี้อาจเกิดจากการเบี่ยงเบนทางพันธุกรรมและการสัมผัสกับสภาพแวดล้อมที่หลากหลายสำหรับประชากรย่อยในประเทศจีนในระยะยาว
อ้างอิง
วู, จี้คุน และคณะ“ความแปรปรวนเชิงโครงสร้างของประชากรจีน และผลกระทบต่อฟีโนไทป์ โรค และการปรับตัวของประชากร”bioRxiv(2021).
ข่าวสารและไฮไลท์ มุ่งหวังที่จะแบ่งปันกรณีศึกษาที่ประสบความสำเร็จล่าสุดกับ Biomarker Technologies เพื่อรวบรวมความสำเร็จทางวิทยาศาสตร์ใหม่ๆ รวมถึงเทคนิคที่โดดเด่นที่นำไปใช้ในระหว่างการศึกษา
เวลาโพสต์: Jan-06-2022

