РЕСЕКУЕНИНГ ЦЕО ГЕНОМ

Геномско праћење САРС-ЦоВ-2 открива варијанту брисања Нсп1 која модулира одговор интерферона типа И
Нанопоре |Иллумина |Поновно секвенцирање целог генома |метагеномика |РНА-Сек |Сангер
Биомаркер Тецхнологиес је пружио техничку подршку за секвенцирање узорака у овој студији.
Хигхлигхтс
1. Секвенцирање генома САРС-ЦоВ-2 и филогнетска анализа идентификују 35 рекурентних мутација укључујући 31 СНП и 4 Индела.
2. Повезивање са 117 клиничких фенотипова открива потенцијално
важне мутације.
∆500-532 у региону кодирања Нсп1 корелира са нижим вирусом
3. оптерећење и серумски ИФН-β.
4. Изолати вируса са мутацијом ∆500-532 индукују нижи ИФН-И
одговор у зараженим ћелијама.
Експериментални дизајн

Достигнућа
1. Епидемиолошки и геномски надзор ЦОВИД-19
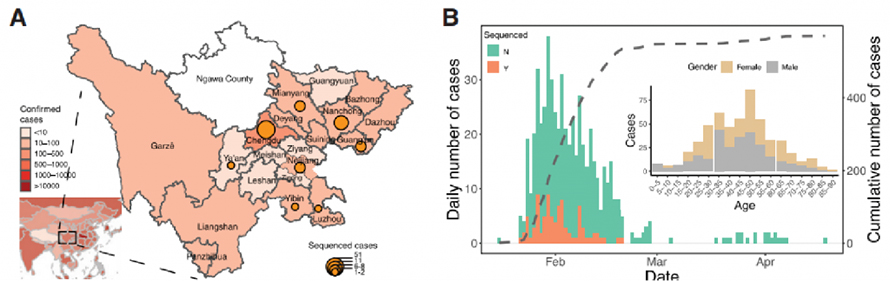
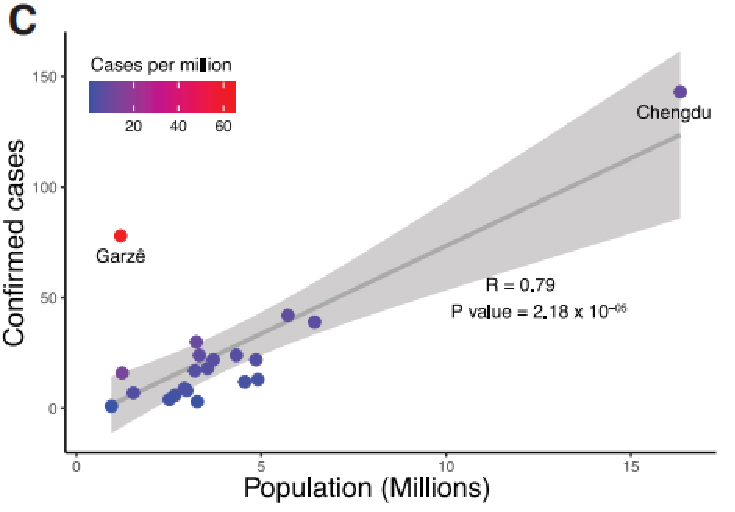
Клинички подаци прикупљени су у провинцији Сечуан у Кини током периода епидемије од 22. јануара 2020. до 20. фебруара 2020. Укупно 538 случајева ЦОВИД-19 потврђено је кПЦР тестовима у Сечуану, од којих је 28,8% било из провинције главни град.Потврђени случајеви у Сечуану су експоненцијално порасли, достижући врхунац 30. јануара.Такође, подаци су потврдили да социјално дистанцирање може бити кључни фактор у спречавању ширења вируса.
Слика 1. Епидемиолошка студија ЦОВИД-19 у провинцији Сечуан, Кина
2. Конструкција генома САРС-ЦоВ-2 и идентификација варијанти
Са мултиплекс ПЦР амплификацијом праћеном секвенцирањем нанопора, генерисано је укупно 310 скоро или делимично комплетних генома од 248 пацијената са прибл.80% генома покривено је са 10 очитавања (средња дубина: 0,39 М читања по узорку).
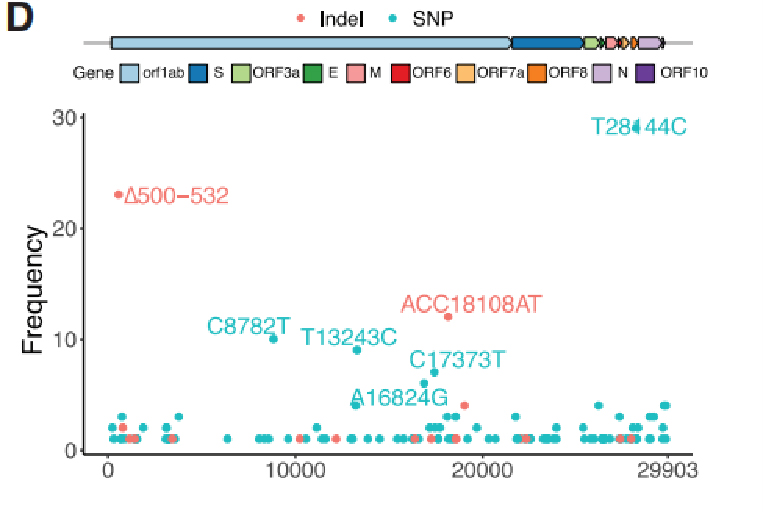
Слика 2. Учесталост сваке варијанте у кохорти Сечуана
Из генома САРС-ЦоВ-2 идентификовано је укупно 104 СНП-а и 18 Индела, у којима су 31 СНП-а и 4 Индела идентификоване као рекурентне генетске варијанте.Упоређујући их са 169 узорака из Вухана и са 81.391 висококвалитетним секвенцама јавног генома у ГИСАИД-у, 29 од 35 пронађених варијанти представљено је на другим континентима.Значајно је да су четири варијанте, укључујући ∆500-532, АЦЦ18108АТ, ∆729-737 и Т13243Ц, пронађене само у Сечуану и Вухану и одсутне у подацима ГИСАИД-а, што указује да је врло вероватно да ће ове варијанте бити импротиране из Вухана, који испуњава путне евиденције пацијената.
Еволуциона анализа са методом максималне вероватноће (МЛ) и приступима Бајесовог молекуларног сата обрађена је на 88 нових вируса из Сечуана и 250 курираних генома из других региона.Геноми са ∆500-532 (делеције у области кодирања Нсп1) пронађени су ретко распоређени у филогенетском стаблу.Анализа хаплотипа на варијантама Нсп1 идентификовала је њих 5 из више градова.Ови резултати сугеришу да се ∆500-532 појавио у више градова и да би могао бити увезен више пута из Вухана.
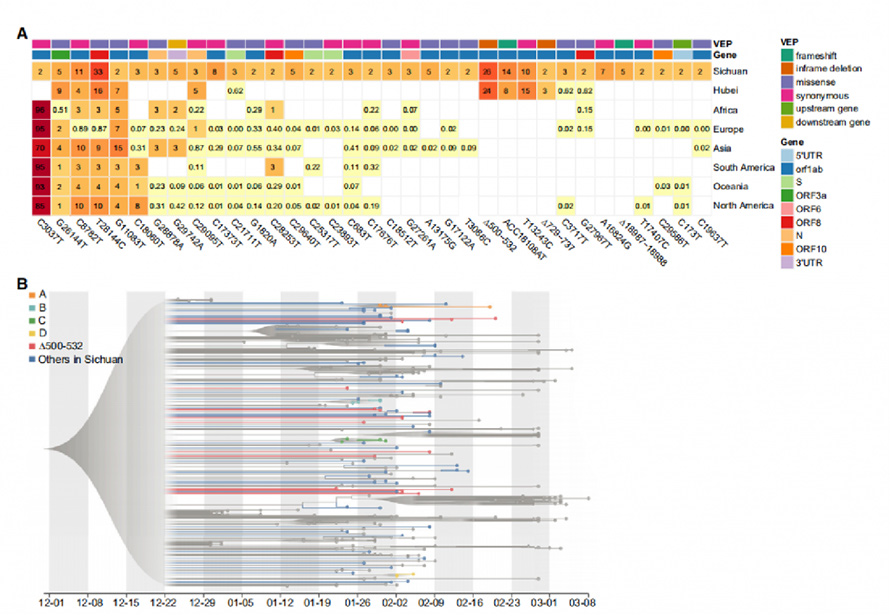
Слика 2. Рекурентне генетске варијанте и филогенетска анализа у геномима САРС-ЦоВ-2
3. Повезивање рекурентних генетских варијанти са клиничким импликацијама
117 клиничких фенотипова је повезано са тежином ЦОВИД-19, при чему је 19 фенотипова повезаних са озбиљношћу класификовано у тешке и не-тешке особине.Однос између ових особина и 35 рекурентних генетских варијанти је визуелизован у би-кластер топлотној мапи.Анализа обогаћивања слична ГСЕА показала је да је ∆500-532 у негативној корелацији са ЕСР, серумским ИФН-β и ЦД3+ЦД8+ Т ћелија у крви.Штавише, кПЦР тестови су показали да пацијенти инфицирани вирусом ∆500-532 имају највећу вредност Цт, односно најниже вирусно оптерећење.
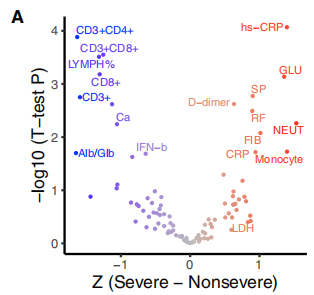
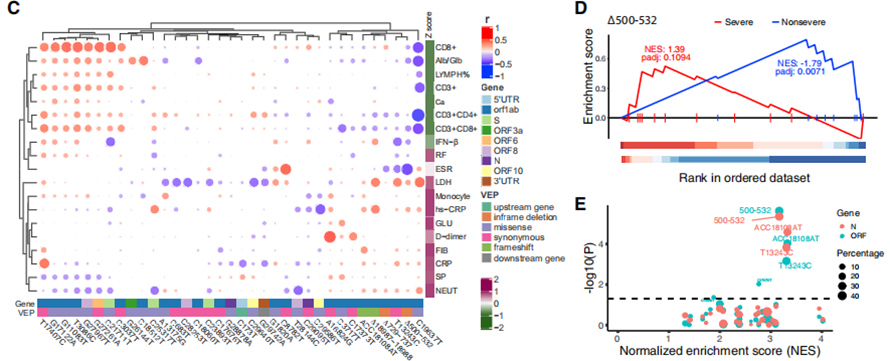
Слика 3. Асоцијације 35 рекурентних генетских варијанти са клиничким фенотиповима
4. Валидација клиничких фенотипова повезаних са вирусном мутацијом
Да би се разумели утицаји ∆500-532 на функције Нсп1, ћелије ХЕК239Т су трансфектоване плазмидима који експримирају пуну дужину, ВТ Нсп1 и мутантне форме са делецијама.Профили транскриптома сваке третиране ХЕК239Т ћелије су обрађени за ПЦА анализу, показујући да су делецијски мутанти груписани релативно ближе и да су се значајно разликовали од ВТ Нсп1.Гени који су значајно појачани код мутаната су углавном обогаћени „биосинтетичким/метаболичким процесом пептида“, „биогенезом комплекса рибонуклеопротеина“, „циљањем протеина на мембрану/ЕР“, итд. Штавише, две делеције су показале различит образац експзије из ВТ.
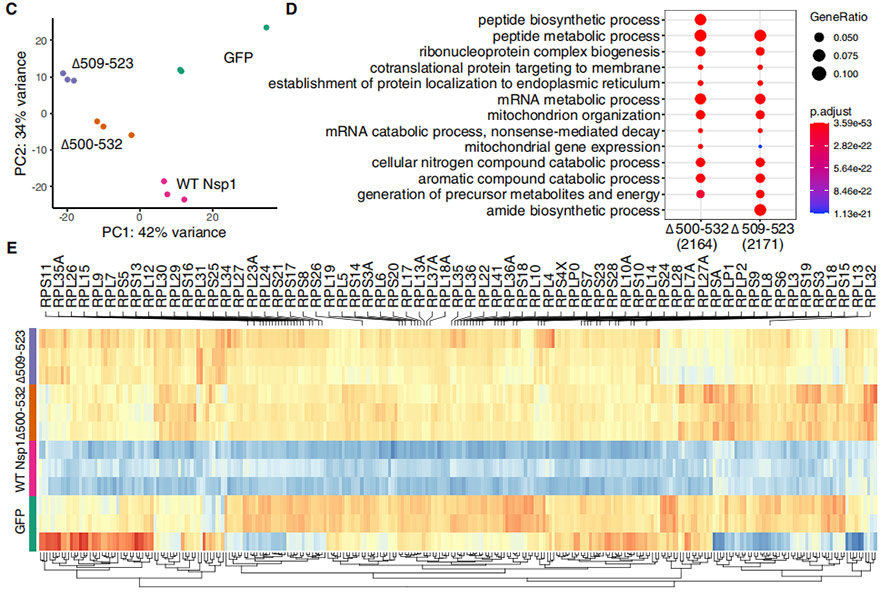
Слика 4. Анализа транскриптома на ћелијама ХЕК239Т трансфектованим помоћу ВТ Нсп1 и оне са брисањем
Утицај делеција на ИФН-1 одговор је такође тестиран у претерано израженој студији.Показало се да сва тестирана брисања смањују одговор ИФН-1 у трансфектованим ћелијама ХЕК239Т и А549 и на нивоу транскриптома и на нивоу протеина.Занимљиво је да су значајно смањени гени у делецијама обогаћени „одбрамбеним одговором на вирус“, „репликацијом вирусног генома“, „регулацијом транскрипције помоћу РНК полимеразе ИИ“ и „одговором на интерферон типа И“.
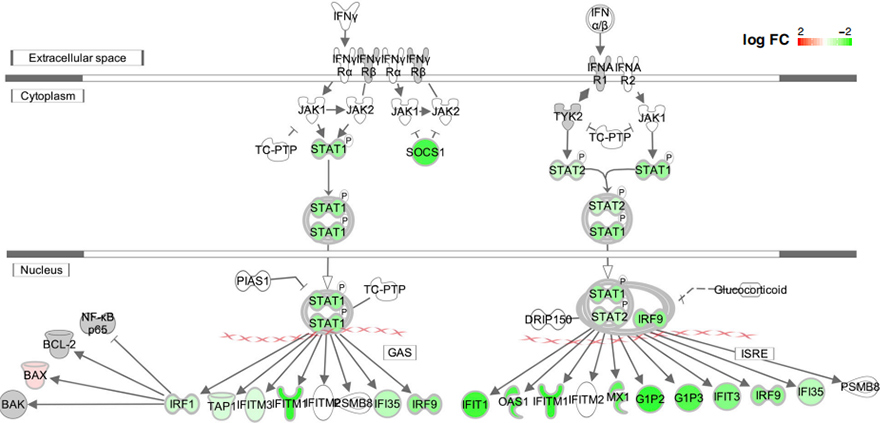
Слика 5. Регулација наниже сигналних путева интерферона код мутанта ∆500-532
У овој студији, утицај ових делеција на вирус је додатно потврђен студијама вирусних инфекција.Вируси са одређеним мутантима су изоловани из клиничких узорака и инфицирани у Цалу-3 ћелије.Детаљни резултати истраживања вирусне инфекције могу се прочитати у раду.
дои:10.1016/ј.чом.2021.01.015
Референце
Лин Ј, Танг Ц, Веи Х, ет ал.Геномски мониторинг САРС-ЦоВ-2 открива варијанту делеције Нсп1 која модулира одговор интерферона типа И[Ј].Ћелијски домаћин и микроб, 2021.
Вести и најважније ствари има за циљ да подели најновије успешне случајеве са Биомаркер Тецхнологиес, ухвати нова научна достигнућа, као и истакнуте технике примењене током студије.
Време поста: Јан-06-2022

