TELJES GENÓM UTASÍTÁSA

A SARS-CoV-2 genomikai megfigyelése egy Nsp1 deléciós változatot tár fel, amely modulálja az I. típusú interferonválaszt
Nanopore |Illumina |A teljes genom újraszekvenálása |metagenomika |RNS-Seq |Sanger
A Biomarker Technologies technikai támogatást nyújtott a mintaszekvenáláshoz ebben a tanulmányban.
Kiemelések
1. A SARS-CoV-2 genom szekvenálása és filogenetikai elemzése 35 visszatérő mutációt azonosít, köztük 31 SNP-t és 4 Indelt.
2. A 117 klinikai fenotípussal való kapcsolat potenciálisan feltárja
fontos mutációk.
A ∆500-532 az Nsp1 kódoló régióban korrelál az alacsonyabb vírussal
3.terhelés és szérum IFN-β.
4. A ∆500-532 mutációt tartalmazó vírusizolátumok alacsonyabb IFN-I-t indukálnak
válasz a fertőzött sejtekben.
Kísérleti terv

Eredmények
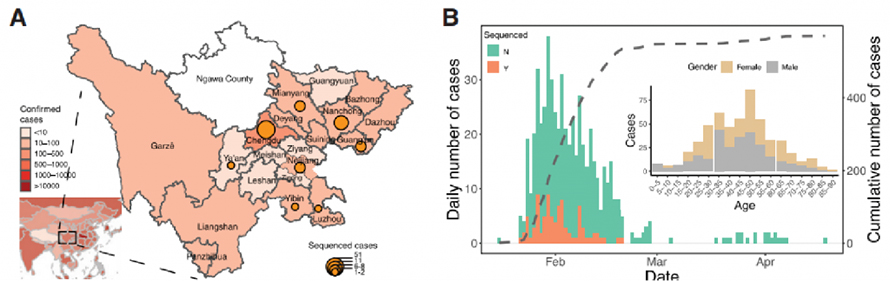
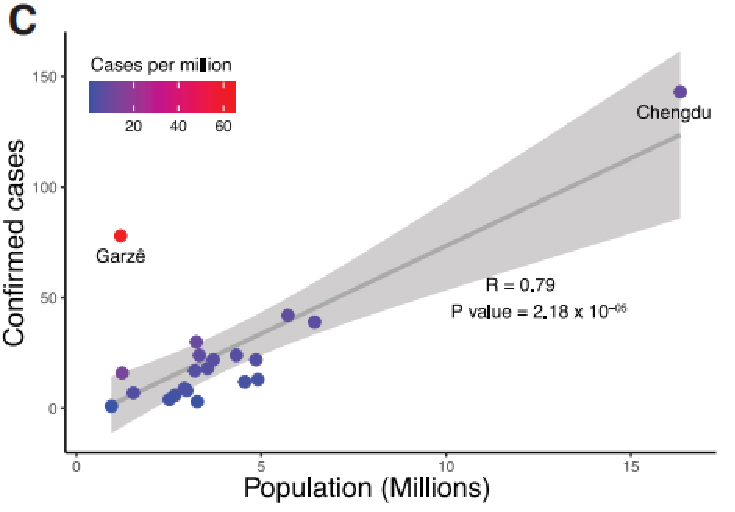
1. COVID-19 járványügyi és genomikai felügyelet
A klinikai adatokat a kínai Szecsuán tartományban gyűjtötték a 2020. január 22. és 2020. február 20. közötti járványkitörési időszakban. Összesen 538 COVID-19 esetet erősítettek meg Szecsuánban a qPCR-tesztek, amelyek 28,8%-a a tartományból származott. főváros.Szecsuánban exponenciálisan nőtt a megerősített esetek száma, és január 30-án érte el a csúcsot.Az adatok azt is alátámasztották, hogy a társadalmi távolságtartás kulcsfontosságú tényező lehet a vírus terjedésének megakadályozásában.
1. ábra: A COVID-19 epidemiológiai vizsgálata Szecsuán tartományban, Kínában
2. SARS-CoV-2 genom konstrukció és variánsok azonosítása
Multiplex PCR amplifikációval, majd nanopórus szekvenálással összesen 310 majdnem vagy részlegesen teljes genomot hoztak létre 248 betegből kb.A genomok 80%-át 10 leolvasás fedi le (átlagos mélység: 0,39 M leolvasás mintánként).
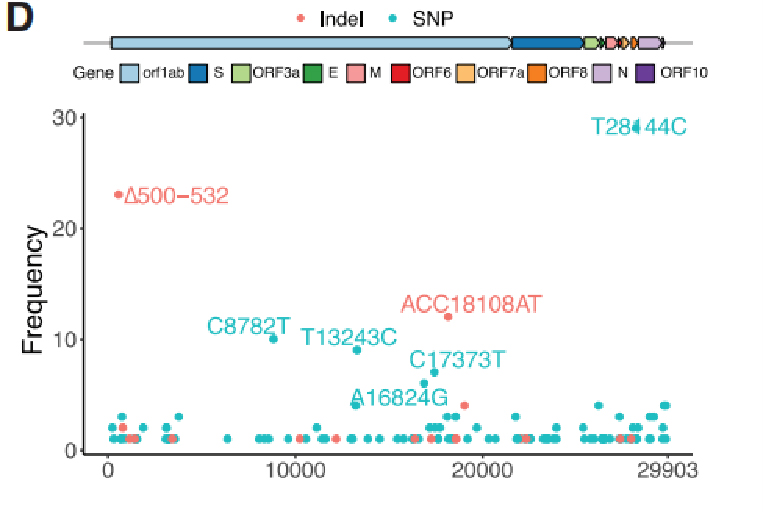
2. ábra: Az egyes változatok gyakorisága a szecsuáni kohorszban
A SARS-CoV-2 genomokból összesen 104 SNP-t és 18 Indelt azonosítottak, amelyekben 31 SNP-t és 4 Indelt azonosítottak visszatérő genetikai variánsként.Összehasonlítva őket 169 vuhani mintával és 81 391 kiváló minőségű nyilvános genomszekvenciával a GISAID-ben, a talált 35 variáns közül 29 más kontinensen is bemutatkozott.Négy változat, köztük a ∆500-532, az ACC18108AT, a ∆729-737 és a T13243C, csak Szecsuánban és Vuhanban volt jelen, és hiányzik a GISAID-adatokból, ami azt jelzi, hogy ezek a változatok nagy valószínűséggel Wuhanból kerültek ki, amelyek megfelelnek a követelményeknek. a betegek utazási nyilvántartásai.
A maximum likelihood (ML) módszerrel és bayesi molekuláris óra megközelítéssel végzett evolúciós elemzést 88 új szecsuáni víruson és 250 más régiókból származó kurált genomon dolgozták fel.A ∆500-532-es genomokat (deléciók az Nsp1 kódoló régióban) ritkán találtuk a filogenetikai fában.Az Nsp1 variánsokon végzett haplotípus-analízis ötöt azonosított több városból.Ezek az eredmények azt sugallták, hogy a ∆500-532 több városban is előfordult, és többször is importálhatták Vuhanból.
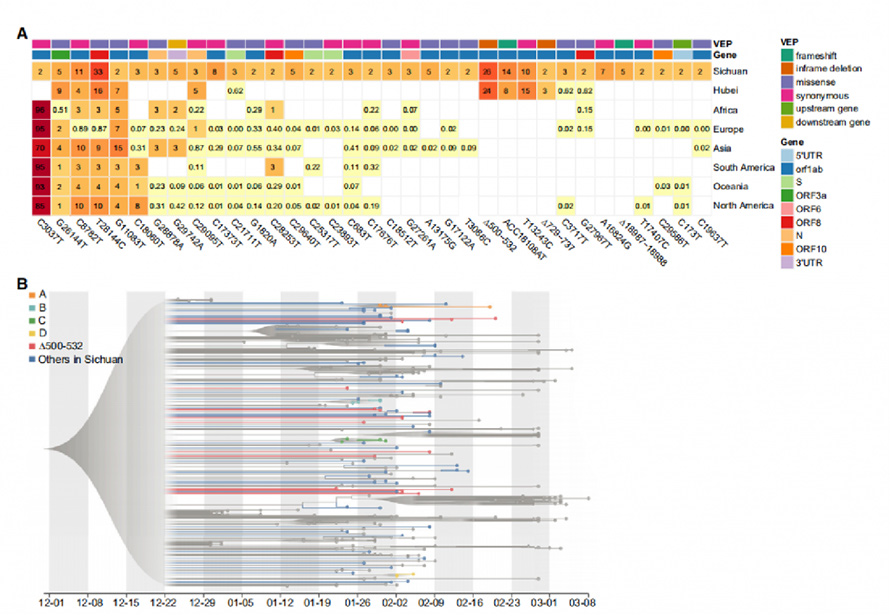
2. ábra: Ismétlődő genetikai variánsok és filogenetikai elemzés a SARS-CoV-2 genomokban
3. Rekurrens genetikai variánsok klinikai vonatkozású asszociációja
117 klinikai fenotípust társítottak a COVID-19 súlyosságához, ahol 19, a súlyossággal összefüggő fenotípust súlyos és nem súlyos tulajdonságokba soroltak.E tulajdonságok és 35 visszatérő genetikai variáns közötti kapcsolatot biklaszteres hőtérképen vizsgáltuk.Egy GSEA-szerű rangsorolt dúsítási analízis kimutatta, hogy a ∆500-532 negatívan korrelál az ESR-rel, a szérum IFN-β és CD3+CD8+ T-sejtszámmal a vérben.Ezenkívül a qPCR tesztek kimutatták, hogy a ∆500-532 vírussal fertőzött betegeknél volt a legmagasabb Ct, azaz a legalacsonyabb a vírusterhelés.
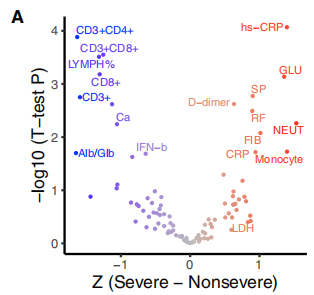
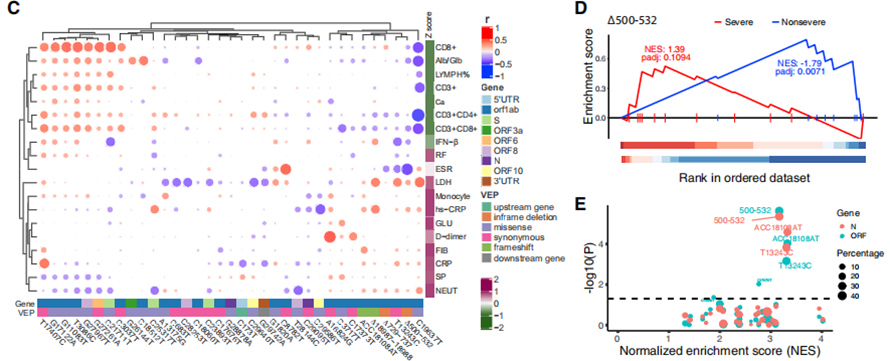
3. ábra: 35 visszatérő genetikai variáns összefüggései klinikai fenotípusokkal
4. A vírusmutációval összefüggő klinikai fenotípusok validálása
Annak érdekében, hogy megértsük a ∆500-532 hatását az Nsp1 funkciókra, HEK239T sejteket transzfektáltunk teljes hosszúságú, WT Nsp1 és deléciós mutáns formákat expresszáló plazmidokkal.Az egyes kezelt HEK239T sejtek transzkriptomprofiljait PCA analízishez feldolgoztuk, ami azt mutatja, hogy a deléciós mutánsok viszonylag közelebb csoportosultak, és szignifikánsan különböznek a WT Nsp1-től.A mutánsokban szignifikánsan felszabályozott gének főként „peptid bioszintetikus/metabolikus folyamatban”, „ribonukleoprotein komplex biogenezisben”, „membránba/ER-be történő fehérje célzásban” stb. gazdagodtak. Ezen túlmenően két deléció a WT-től eltérő expziós mintát mutatott.
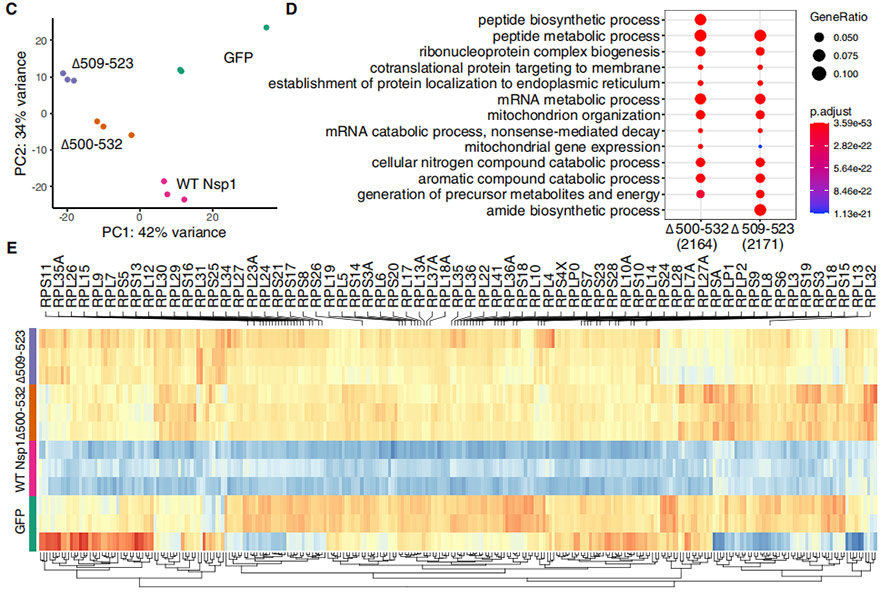
4. ábra: WT Nsp1-gyel transzfektált és deléciós HEK239T-sejtek transzkriptomaanalízise
A delécióknak az IFN-1 válaszra gyakorolt hatását túlexpresszált vizsgálatban is tesztelték.Kimutatták, hogy az összes tesztelt deléció csökkenti az IFN-1 reakciót a transzfektált HEK239T és A549 sejtekben mind a transzkriptom, mind a fehérje szinten.Érdekes módon a jelentős mértékben leszabályozott gének a deléciókban gazdagodtak a „vírus elleni védekezési válaszban”, a „vírus genom replikációjában”, „az RNS-polimeráz II-es transzkripció szabályozásában” és az „I-es típusú interferonra adott válaszban”.
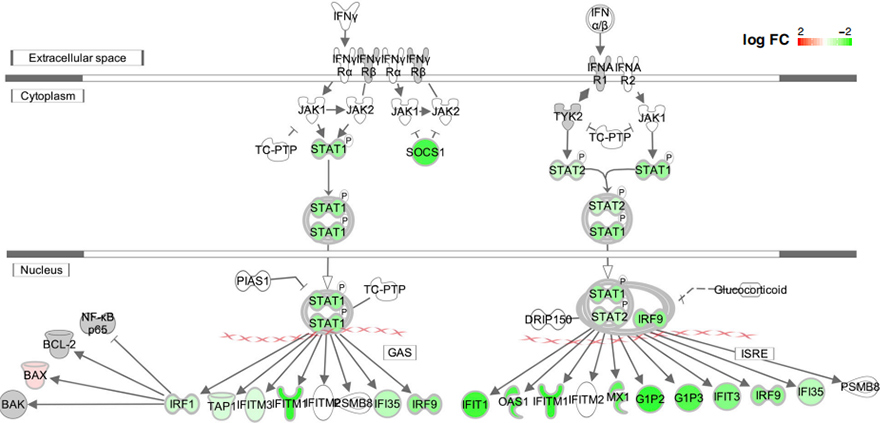
5. ábra: Az interferon jelátviteli útvonalak leszabályozása ∆500-532 mutánsban
Ebben a vizsgálatban ezeknek a delécióknak a vírusra gyakorolt hatását vírusfertőzési vizsgálatok is megerősítették.Bizonyos mutánsokat tartalmazó vírusokat klinikai mintákból izoláltunk, és Calu-3 sejteket fertőztünk meg.A vírusfertőzés vizsgálatának részletes eredményei a lapban olvashatók.
doi:10.1016/j.chom.2021.01.015
Referencia
Lin J, Tang C, Wei H és mtsai.A SARS-CoV-2 genomiális monitorozása egy Nsp1 deléciós változatot tár fel, amely modulálja az I. típusú interferonválaszt[J].Sejtgazda és mikroba, 2021.
Hírek és kiemelések célja a legújabb sikeres esetek megosztása a Biomarker Technologies vállalattal, megörökítve az új tudományos eredményeket, valamint a tanulmány során alkalmazott kiemelkedő technikákat.
Feladás időpontja: 2022-06-06

