دنبال کردن کل ژنوم

پایش ژنومیک SARS-CoV-2 یک نوع حذف Nsp1 را نشان می دهد که پاسخ اینترفرون نوع I را تعدیل می کند.
نانو حفره |ایلومینا |توالی یابی کل ژنوم |متاژنومیکس |RNA-Seq |سنگر
Biomarker Technologies پشتیبانی فنی را در مورد توالی یابی نمونه در این مطالعه ارائه کرد.
نکات برجسته
1. توالی یابی ژنوم SARS-CoV-2 و تجزیه و تحلیل فیلوژنتیک، 35 جهش عودکننده شامل 31 SNP و 4 ایندل را شناسایی می کند.
2. ارتباط با 117 فنوتیپ بالینی بالقوه را نشان می دهد
جهش های مهم
∆500-532 در ناحیه کدکننده Nsp1 با ویروسی پایینتر ارتباط دارد
3. بار و IFN-β سرم.
4. ایزوله های ویروسی با جهش ∆500-532 باعث کاهش IFN-I می شوند.
پاسخ در سلول های آلوده
طراحی تجربی

دستاوردها
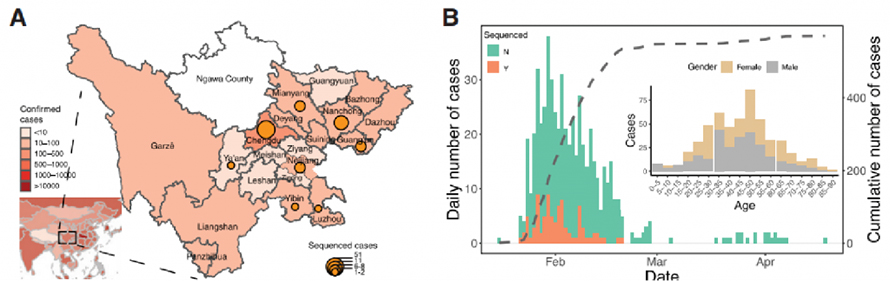
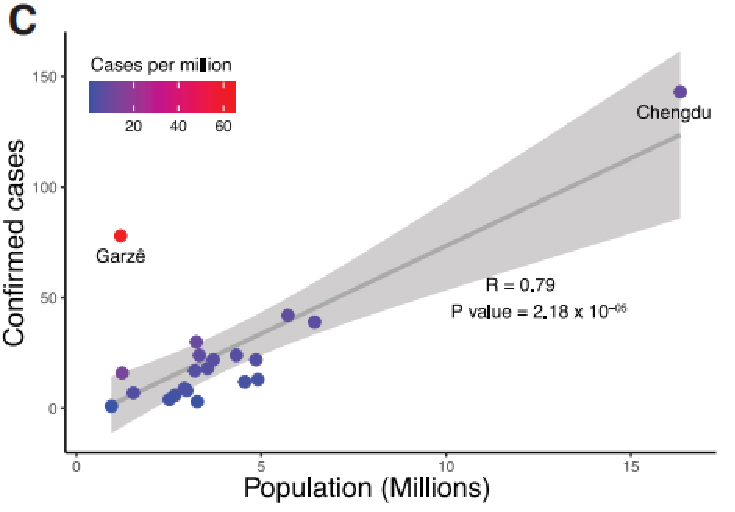
1. نظارت اپیدمیولوژیک و ژنومیک COVID-19
دادههای بالینی در استان سیچوان، چین در طول دوره شیوع از 22 ژانویه 2020 تا 20 فوریه 2020 جمعآوری شد. در مجموع 538 مورد COVID-19 توسط آزمایشهای qPCR در سیچوان تأیید شد که 28.8 درصد از آنها از استان بودند. سرمایه، پایتخت.موارد تایید شده در سیچوان به طور تصاعدی افزایش یافت و در 30 ژانویه به اوج خود رسید.همچنین، داده ها نشان می دهد که فاصله گذاری اجتماعی می تواند یک عامل کلیدی در جلوگیری از انتشار ویروس باشد.
شکل 1. مطالعه اپیدمیولوژیک COVID-19 در استان سیچوان، چین
2. ساختار ژنوم SARS-CoV-2 و شناسایی انواع آن
با تکثیر مالتی پلکس PCR و به دنبال آن توالی یابی نانوحفره، در مجموع 310 ژنوم تقریباً یا جزئی کامل از 248 بیمار با حدوداً تولید شد.80 درصد از ژنوم ها با 10 خواندن پوشش داده شده اند (میانگین عمق: 0.39 M خواندن در هر نمونه).
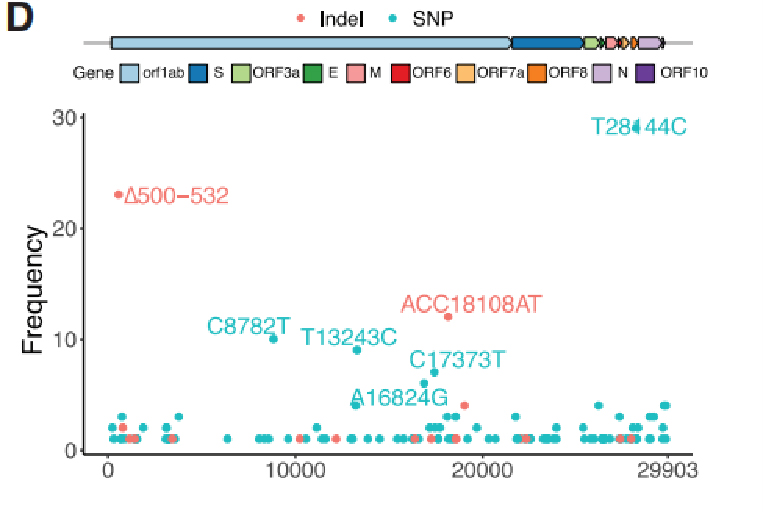
شکل 2. فراوانی هر گونه در گروه سیچوان
در مجموع 104 SNP و 18 ایندل از ژنوم SARS-CoV-2 شناسایی شد که در آن ها 31 SNP و 4 Indels به عنوان واریانت های ژنتیکی مکرر شناسایی شدند.با مقایسه آنها با 169 نمونه از ووهان و با 81391 توالی ژنوم عمومی با کیفیت بالا در GISAID، 29 مورد از 35 نوع یافت شده در سایر قاره ها ارائه شده است.قابل ذکر است، چهار نوع از جمله ∆500-532، ACC18108AT، ∆729-737 و T13243C، فقط در سیچوان و ووهان وجود داشتند و در دادههای GISAID وجود نداشتند، که نشان میدهد این گونهها به احتمال زیاد از ووهان که مطابق با استانداردهای جهانی است، ایجاد شدهاند. سوابق سفر بیماران
تجزیه و تحلیل تکاملی با روش حداکثر احتمال (ML) و رویکردهای ساعت مولکولی بیزی روی 88 ویروس جدید از سیچوان و 250 ژنوم انتخاب شده از مناطق دیگر پردازش شد.ژنومهایی با ∆500-532 (حذفها در ناحیه کدکننده Nsp1) بهطور پراکنده در درخت فیلوژنتیک توزیع شدند.تجزیه و تحلیل هاپلوتیپ بر روی انواع Nsp1، 5 مورد از آنها را از چندین شهر شناسایی کرد.این نتایج نشان داد که ∆500-532 در چندین شهر رخ داده است و ممکن است چندین بار از ووهان وارد شود.
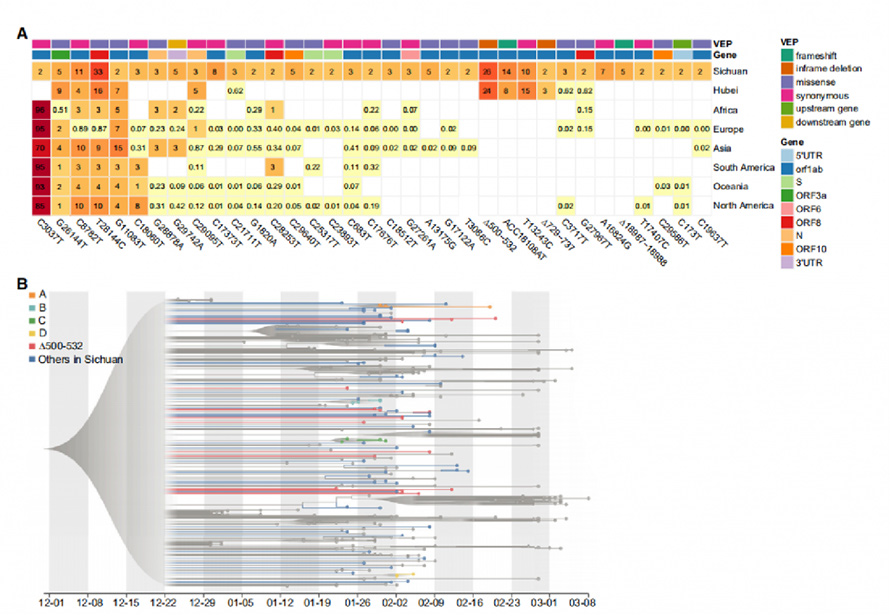
شکل 2. انواع ژنتیکی مکرر و تجزیه و تحلیل فیلوژنتیک در ژنوم SARS-CoV-2
3. ارتباط انواع ژنتیکی مکرر با پیامدهای بالینی
117 فنوتیپ بالینی با شدت کووید-19 مرتبط بودند، که در آن 19 فنوتیپ مرتبط با شدت به صفات شدید و غیر شدید طبقهبندی شدند.ارتباط بین این صفات و 35 گونه ژنتیکی مکرر در نقشه حرارتی دو خوشه ای زنده شد.تجزیه و تحلیل غنیسازی رتبهبندی شده مشابه GSEA نشان داد که ∆500-532 با ESR، IFN-β سرم و تعداد سلولهای T CD3+CD8+ در خون همبستگی منفی دارد.علاوه بر این، آزمایشهای qPCR نشان داد که بیماران آلوده به ویروس حاوی ∆500-532 دارای بالاترین مقدار Ct، یعنی کمترین بار ویروسی بودند.
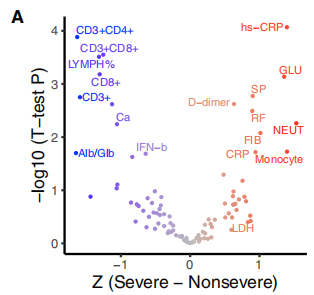
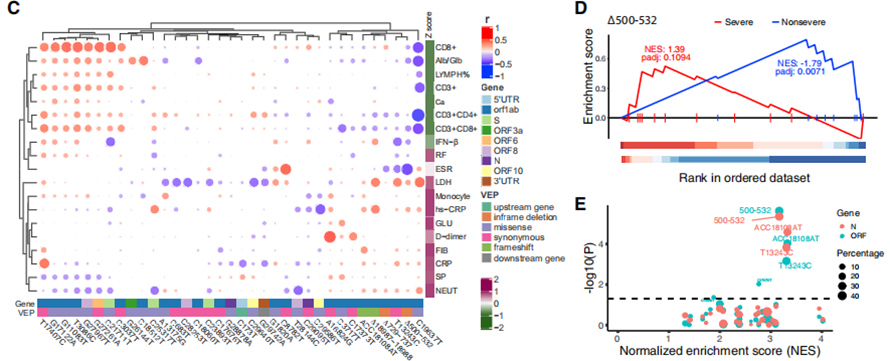
شکل 3. ارتباط 35 گونه ژنتیکی راجعه با فنوتیپ های بالینی
4. اعتبار سنجی فنوتیپ های بالینی مرتبط با جهش ویروسی
به منظور درک تأثیر ∆500-532 بر عملکردهای Nsp1، سلولهای HEK239T با پلاسمیدهایی که تمام طول، WT Nsp1 و اشکال جهش یافته با حذف را بیان میکنند، ترانسفکت شدند.نمایههای رونوشت هر سلول HEK239T تیمار شده برای تجزیه و تحلیل PCA پردازش شد، که نشان میدهد جهشهای حذف نسبتاً نزدیکتر هستند و به طور قابلتوجهی با WT Nsp1 متفاوت هستند.ژنهایی که به طور قابلتوجهی در جهشیافتهها تنظیم مثبت شدند، عمدتاً در «فرایند بیوسنتزی/متابولیک پپتیدی»، «بیوژنز کمپلکس ریبونوکلئوپروتئین»، «هدفگیری پروتئین به غشاء/ER» و غیره غنی شدند.
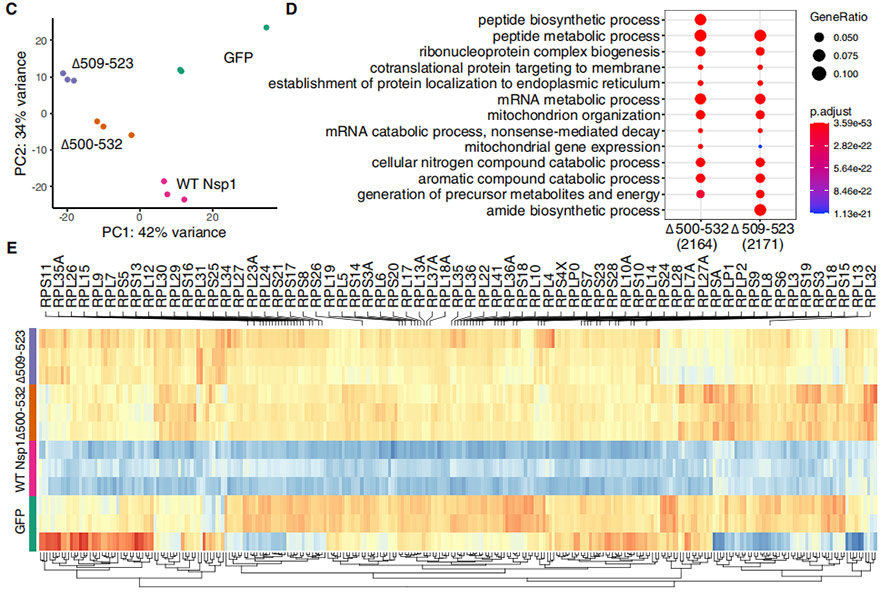
شکل 4. تجزیه و تحلیل رونوشت بر روی سلول های HEK239T ترانسفکت شده توسط WT Nsp1 و با حذف
تأثیر حذف ها بر پاسخ IFN-1 نیز در مطالعه با بیان بیش از حد مورد آزمایش قرار گرفت.نشان داده شد که تمام حذفهای آزمایششده واکنش IFN-1 را در سلولهای HEK239T و A549 ترانسفکتشده در سطح رونوشت و پروتئین کاهش میدهند.جالب توجه است که ژنهای با کاهش قابل توجهی در حذفها در «پاسخ دفاعی به ویروس»، «تکثیر ژنوم ویروسی»، «تنظیم رونویسی توسط RNA پلیمراز II» و «پاسخ به اینترفرون نوع I» غنی شدهاند.
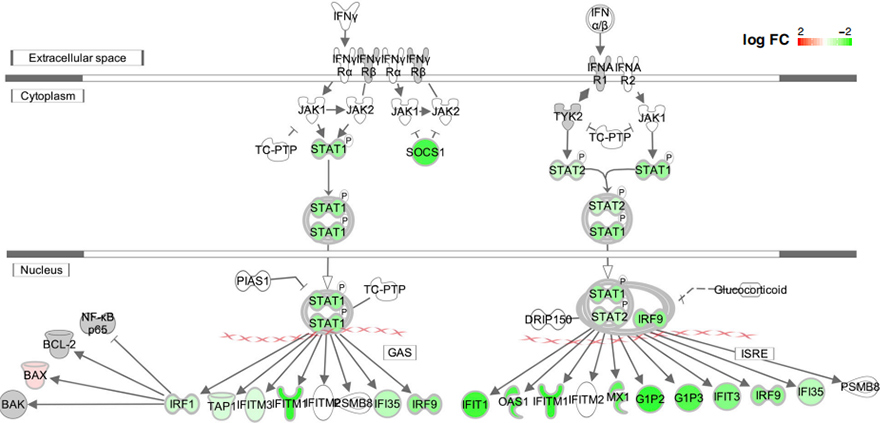
شکل 5. تنظیم پایین مسیرهای سیگنال دهی اینترفرون در جهش 500-532 ∆500
در این مطالعه، تاثیر این حذف ها بر روی ویروس توسط مطالعات عفونت ویروسی بیشتر تایید شد.ویروسهایی با جهشهای خاص از نمونههای بالینی جدا شده و به سلولهای Calu-3 آلوده شدند.نتایج دقیق در مورد مطالعه عفونت ویروسی را می توان در مقاله خواند.
doi:10.1016/j.chom.2021.01.015
ارجاع
لین جی، تانگ سی، وی اچ، و همکاران.پایش ژنومیک SARS-CoV-2 یک نوع حذف Nsp1 را نشان می دهد که پاسخ اینترفرون نوع I [J] را تعدیل می کند.میزبان سلولی و میکروب، 2021.
اخبار و نکات مهم هدف آن به اشتراک گذاری آخرین موارد موفق با Biomarker Technologies، ثبت دستاوردهای علمی جدید و همچنین تکنیک های برجسته به کار رفته در طول مطالعه است.
زمان ارسال: ژانویه-06-2022

