Паўторнае секвеніраванне поўнага геному

Структурныя варыянты кітайскай папуляцыі і іх уплыў на фенатыпы, захворванні і адаптацыю насельніцтва
Нанапор |PacBio |Паўторная паслядоўнасць геному |Выклік структурнай варыяцыі
У гэтым даследаванні секвенирование Nanopore PromethION было прадастаўлена Biomarker Technologies.
Асноўныя моманты
У гэтым даследаванні агульны пейзаж структурных варыяцый (SV) у геноме чалавека быў выяўлены з дапамогай доўгачытанага секвеніравання на платформе Nanopore PromethION, што паглыбляе разуменне SV ў фенатыпах, захворваннях і эвалюцыі.
Эксперыментальны дызайн
Узоры: лейкацыты перыферычнай крыві 405 нероднасных кітайцаў (206 мужчын і 199 жанчын) з 68 фенатыпічнымі і клінічнымі вымярэннямі.Сярод усіх асобін рэгіёны продкаў 124 асобін былі правінцыямі на поўначы, 198 асобін - на поўдні, 53 - на паўднёвым захадзе і 30 - невядомыя.
Стратэгія секвенирования: секвенирование доўгага счытвання ўсяго геному (LRS) са счытваннем Nanopore 1D і счытваннем PacBio HiFi.
Платформа секвенирования: Nanopore PromethION;Працяг PacBio II
Выклік змены структуры
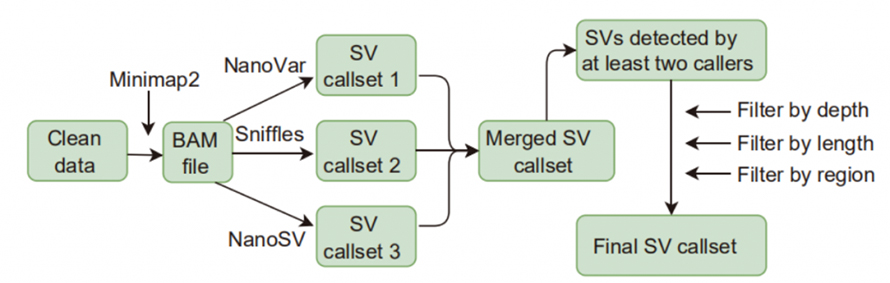
Малюнак 1. Рабочы працэс выкліку і фільтрацыі SV
Асноўныя дасягненні
Выяўленне і праверка варыяцый структуры
Набор дат Nanopore: у агульнай складанасці 20,7 ТБ чыстых чытанняў, згенераваных на платформе секвенирования PromethION, у сярэднім 51 ГБ даных на выбарку, прыбл.17-кратная глыбіня.
Выраўноўванне эталоннага геному (GRCh38): Дасягнута сярэдняя частата адлюстравання 94,1%.Сярэдняя частата памылак (12,6%) была падобная да папярэдняга параўнальнага даследавання (12,6%) (малюнкі 2b і 2c)
Выклік змены структуры (SV): выклікаючыя SV, якія выкарыстоўваліся ў гэтым даследаванні, уключалі Sniffles, NanoVar і NanoSV.SV з высокім упэўненасцю вызначаліся як SV, ідэнтыфікаваныя як мінімум двума абанентамі і прайшлі фільтрацыю па глыбіні, даўжыні і вобласці.
У сярэднім у кожным узоры было выяўлена 18 489 (ад 15 439 да 22 505) высоканадзейных SV.(Малюнак 2d, 2e і 2f)
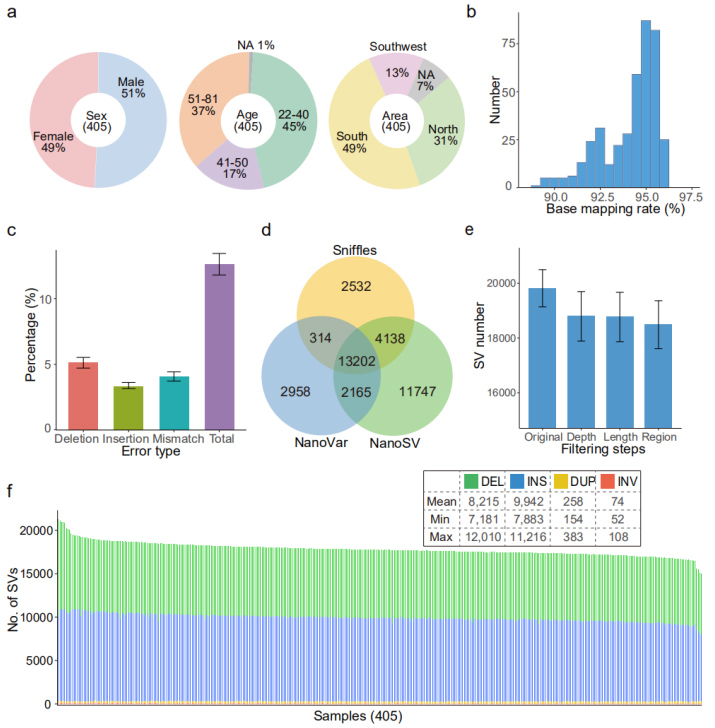
Малюнак 2. Агульны ландшафт SV, вызначаных наборам даных Nanopore
Праверка PacBio: SV, ідэнтыфікаваныя ў адным узоры (HG002, дзіця), былі правераны наборам даных PacBio HiFi.Агульная частата ілжывых адкрыццяў (FDR) склала 3,2%, што сведчыць аб адносна надзейнай ідэнтыфікацыі SV па паказаннях Nanopore.
Нелішнія SV і геномныя асаблівасці
Нерэзерваваныя SV: набор з 132 312 нерэзерваваных SV быў атрыманы шляхам аб'яднання SV ва ўсіх узорах, які ўключае 67 405 DEL, 60 182 INS, 3956 DUP і 769 INV.(Малюнак 3а)
Параўнанне з існуючымі наборамі даных SV: гэты набор даных параўноўваўся з апублікаваным наборам даных TGS або NGS.Сярод чатырох набораў даных, якія параўноўваліся, LRS15, які таксама з'яўляецца адзіным наборам даных з платформы доўгачытанага секвеніравання (PacBio), падзяляў найбольшае супадзенне з гэтым наборам даных.Больш за тое, 53,3% (70 471) SV у гэтым наборы дадзеных былі зарэгістраваныя ўпершыню.Разглядаючы кожны тып SV, колькасць адноўленых INS з наборам даных секвеніравання доўгага счытвання была значна большай, чым колькасць астатніх з кароткім счытваннем, што сведчыць аб тым, што секвеніраванне доўгага счытвання асабліва эфектыўна пры выяўленні INS.(Малюнкі 3b і 3c)
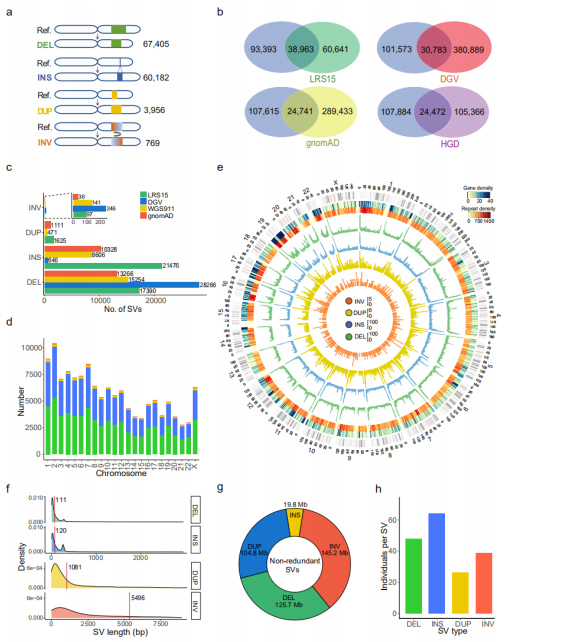
Малюнак 3. Уласцівасці нерэзерваваных SV для кожнага тыпу SV
Геномныя асаблівасці: колькасць SV была значна карэлюе з даўжынёй храмасомы.Размеркаванне генаў, паўтораў, DEL (зялёны), INS (сіні), DUP (жоўты) і INV (аранжавы) былі адлюстраваны на дыяграме Circos, дзе агульнае павелічэнне SV назіралася ў канцы плеч храмасом.(Малюнкі 3d і 3e)
Даўжыня SV: даўжыня INS і DEL аказалася значна карацейшай, чым даўжыня DUP і INV, што супадае з даўжынямі, вызначанымі наборам даных PacBio HiFi.Даўжыня ўсіх выяўленых SV склала 395,6 Мб, што займае 13,2% усяго геному чалавека.SVs закранулі ў сярэднім 23,0 Мб (прыблізна 0,8%) геному на чалавека.(Малюнак 3f і 3g)
Функцыянальнае, фенатыпічнае і клінічнае ўздзеянне SV
Прагназуемая страта функцыі (pLoF) SV: pLoF SV вызначаліся як SV, якія ўзаемадзейнічалі з CDS, дзе кадзіруючыя нуклеатыды былі выдалены або ORF былі зменены.Усяго было анатавана 1929 pLoF SV, якія ўплываюць на CDS 1681 гена.Сярод іх 38 генаў вылучаюць «звязванне з рэцэптарам імунаглабуліну» ў аналізе ўзбагачэння GO.Гэтыя pLoF SV былі дадаткова анатаваны GWAS, OMIM і COSMIC адпаведна.(Малюнкі 4а і 4б)
Фенатыпічнае і клінічна значныя SV: было паказана, што шэраг SV у наборы дадзеных нанапор маюць фенатыпічнае і клінічнае значэнне.Рэдкі гетэразіготны DEL памерам 19,3 кб, які, як вядома, выклікае альфа-таласемію, быў ідэнтыфікаваны ў трох асобін, у якіх парушаныя функцыі генаў субадзінак гемаглабіну альфа 1 і 2 (HBA1 і HBA2).Яшчэ адзін DEL памерам 27,4 кб на гене, які кадуе субадзінак гемаглабіну бэта (HBB), быў ідэнтыфікаваны ў іншага чалавека.Вядома, што гэты SV выклікае сур'ёзныя гемаглабінапатыі.(Малюнак 4c)
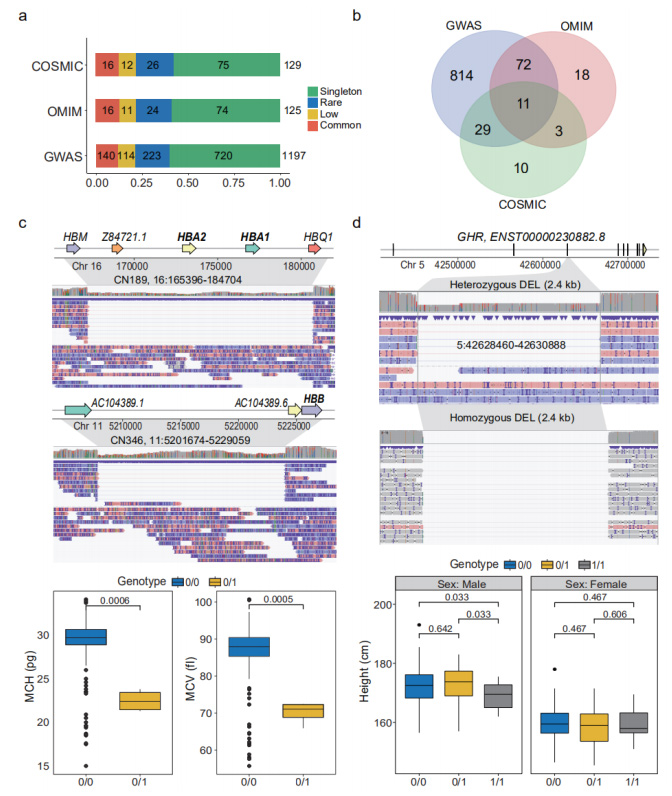
Малюнак 4. pLoF SV, звязаныя з фенатыпамі і захворваннямі
Агульны DEL памерам 2,4 кб назіраўся ў 35 гомазіготных і 67 гетэразіготных носьбітаў, які ахоплівае поўную вобласць 3-га экзона рэцэптара гармону росту (GHR).Гомозиготные носьбіты апынуліся значна меншымі, чым гетерзиготные (p=0,033).(Малюнак 4d)
Акрамя таго, гэтыя SV былі апрацаваны для даследаванняў эвалюцыі насельніцтва паміж дзвюма рэгіянальнымі групамі: Паўночным і Паўднёвым Кітаем.Значна дыферэнцыяльныя SV былі размеркаваны на Chr 1, 2, 3, 6, 10, 12, 14 і 19, у межах якіх верхнія былі звязаны з рэгіёнамі імунітэту, такімі як IGH, MHC і г.д. Разумна выказаць здагадку, што дыферэнцыяцыя ў гэтых SV можа быць з-за генетычнага дрэйфу і доўгатэрміновага ўздзеяння розных асяроддзяў для субпапуляцый у Кітаі.
Даведка
Ву, Чжыкунь і інш.«Структурныя варыянты кітайскай папуляцыі і іх уплыў на фенатыпы, хваробы і адаптацыю насельніцтва».bioRxiv(2021).
Навіны і асноўныя моманты накіравана на абмен апошнімі паспяховымі кейсамі з Biomarker Technologies, фіксаванне новых навуковых дасягненняў, а таксама вядомых метадаў, якія прымяняюцца падчас даследавання.
Час публікацыі: 6 студзеня 2022 г

